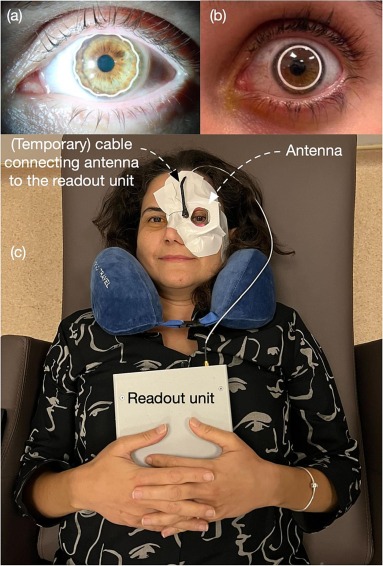
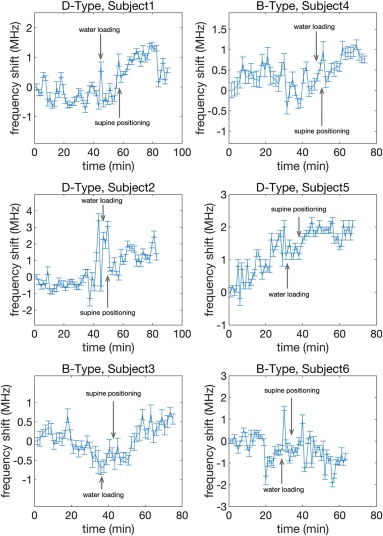
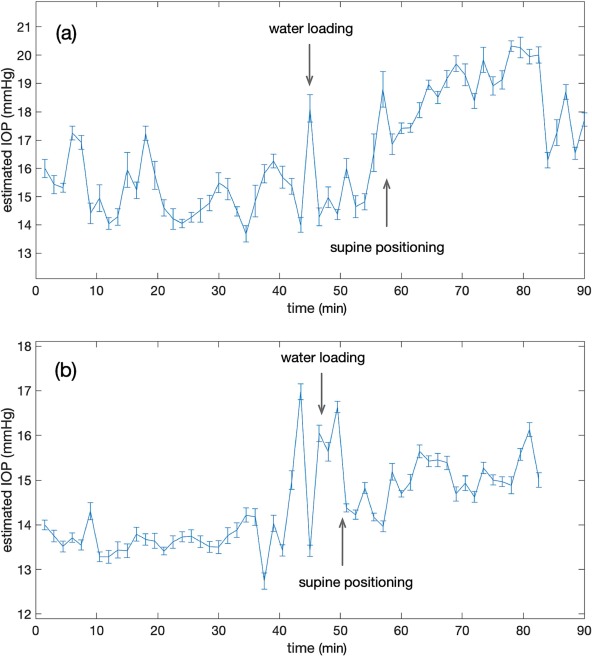
El glaucoma es una de las principales causas de ceguera sin cura conocida, pero un tratamiento temprano y un monitoreo efectivo a menudo pueden frenar la progresión de la enfermedad. El monitoreo del glaucoma se basa en la medición de la presión intraocular (PIO), un parámetro fisiológico relacionado con el estado mecánico y los parámetros del ojo. Convencionalmente, el diagnóstico y la evaluación del progreso del glaucoma se basan en la medición discreta de la PIO en clínicas. Estudios recientes han demostrado la importancia de monitorear continuamente la PIO durante 24 horas para elucidar el efecto del ritmo circadiano. En este trabajo, se presenta un estudio piloto en humanos de un lente de contacto con un sensor integrado inspirado en metamateriales eléctricamente pasivos para monitorear las fluctuaciones de la PIO. El sensor en el lente de contacto es un resonador basado en metamateriales y eléctricamente pasivo, que se puede medir mediante un parche de antena portátil. El sistema se ha probado con seis voluntarios saludables durante un experimento que indujo cambios deliberados en la PIO mediante carga de agua y colocación de los individuos en posición supina utilizando un asiento reclinable. Los datos iniciales, comparados con las mediciones del tonómetro, sugieren que el sistema puede utilizarse para evaluar la variación de la PIO de manera continua.
1. Introducción
El glaucoma afecta a más de 70 millones de personas, estimándose que esa cifra aumentará a más de 110 millones para 2040 [[1]]. Es una condición crónica sin cura y la segunda causa principal de ceguera [[2]]. Con el envejecimiento de la población, especialmente en países desarrollados, la prevalencia del glaucoma también está en aumento [[2]]. La práctica médica actual para el manejo del glaucoma consiste en monitorear la PIO (Presión Intraocular), un parámetro fisiológico crítico que refleja el equilibrio entre la producción y el drenaje del humor acuoso en el ojo. La PIO elevada es un factor de riesgo importante que necesita ser cuantificado y evaluado. Actualmente, la tonometría de aplanación de Goldmann (TAG) es el método más utilizado para medir la PIO en la práctica clínica. Sin embargo, la TAG tiene limitaciones, como su dependencia de las propiedades corneales y su incapacidad para capturar fluctuaciones a corto plazo en la PIO [[3]]. Además, el enfoque convencional es medir la PIO durante una consulta oftalmológica y reducirla mediante el uso de medicamentos y/o cirugía para prevenir una mayor pérdida visual. Sin embargo, este enfoque tiene limitaciones médicas, sociales y económicas evidentes. Medir los niveles de PIO solo durante las visitas al médico e evaluar la progresión de la enfermedad basándose en mediciones únicas en períodos de varios meses impide que los proveedores de atención oftalmológica tomen acciones oportunas y efectivas [[4]].
Un paradigma emergente para la estrategia de medición de la PIO es observar los ciclos circadianos de variación de la PIO en un período de 24 h abarcando un solo día y repetir esta estrategia de medición periódicamente durante un período prolongado [5, 6]. La PIO varía significativamente a lo largo del período circadiano, y estas fluctuaciones y los niveles máximos asociados se han identificado como factores de riesgo para la progresión del glaucoma. Estudios respaldan la hipótesis de que la fluctuación de la PIO debería considerarse como un factor de riesgo independiente para la progresión del glaucoma [[7]]. Obtener conjuntos de datos que capturen ciclos circadianos completos puede conducir a una mejor comprensión de varios parámetros ambientales y fisiológicos que causan la fluctuación de la PIO [[8]]. Las estrategias de tratamiento para el glaucoma se basan en establecer un rango objetivo de PIO en el que se asume que el desarrollo de un daño glaucomatoso adicional se reduce sustancialmente. Recientes recomendaciones clínicas incluyen considerar la fluctuación de la PIO además de la reducción [[9]].
Una estrategia para implementar esta táctica consiste en invitar a los pacientes a clínicas durante un período de 24 horas y medir periódicamente la Presión Intraocular (PIO) mediante métodos de tonometría. Aumentar la frecuencia de las visitas médicas para permitir el monitoreo de los ciclos circadianos no es económicamente viable y podría imponer limitaciones al bienestar de los pacientes. Además, medir la PIO con métodos convencionales de tonometría durante la noche puede generar errores sistemáticos en las mediciones, ya que se ha informado que despertar a los pacientes para mediciones de tonometría nocturnas puede afectar los resultados [10]. No obstante, hay esfuerzos significativos para desarrollar un tonómetro adecuado para uso doméstico, como el iCare, que utiliza la tonometría de rebote [11]. En este enfoque, la sonda está en contacto con el ojo, y los pacientes, generalmente sin capacitación médica, realizan mediciones únicas. Realizar múltiples mediciones durante la noche puede producir datos inexactos, ya que la PIO a menudo aumenta inmediatamente después de despertar a los pacientes [12].
Recientemente, se han introducido varias plataformas de monitoreo continuo de la PIO. Triggerfish de Sensimed es el producto más estudiado, basado en un sensor de deformación incrustado en una lente de contacto [13]. Este producto, que recibió la aprobación de la FDA en 2014, es actualmente el único dispositivo de monitoreo continuo basado en lentes de contacto en el mercado. Triggerfish sigue los cambios en la forma corneal en respuesta a las variaciones de la PIO. Aunque diversos estudios han demostrado la utilidad de este enfoque para rastrear la PIO durante períodos prolongados de manera portátil y no invasiva [13], la tecnología presenta limitaciones, como una débil correlación entre los datos del sistema y las mediciones externas de la PIO [14]. Además, la presencia de un chip de silicio eléctricamente activo en el centro de la lente de contacto puede afectar negativamente su flexibilidad, limitando su capacidad para adaptarse perfectamente al ojo del paciente, lo que podría resultar en imprecisiones en las mediciones. También se destaca que este chip puede restringir el campo de visión del paciente, causando estrés emocional y limitando las actividades diarias.
-
- Konstas A.G.
- et al.
Adv Ther. Nov. 2018; 35: 1775-1804https://doi.org/10.1007/s12325-018-0812-z
- Google Scholar
-
- Da Silva F.
- Lira M.
- Is 24-hour intraocular pressure monitoring necessary in glaucoma?. Semin Ophthalmol. May 2013; 28: 157-164https://doi.org/10.3109/08820538.2013.771201 View in Article
- Circadian fluctuation of mean ocular perfusion pressure is a consistent risk factor for normal-tension glaucoma. Investigative Opthalmology & Visual Science. Jan. 2007; 48: 104https://doi.org/10.1167/iovs.06-0615 View in Article
- IOP telemetry in the nonhuman primate. Exp Eye Res. Dec. 2015; 141: 91-98https://doi.org/10.1016/j.exer.2015.07.015 View in Article
- Intraocular pressure fluctuation: is it important?. J Ophthalmic Vis Res. 2018; 13: 170-174https://doi.org/10.4103/jovr.jovr_35_18 View in Article
- 24-hour Intraocular pressure monitoring: the way ahead. Rom J Ophthalmol. 2019; 63: 315-320 View in Article
- The Icare HOME (TA022) study. Ophthalmology. Aug. 2016; 123: 1675-1684https://doi.org/10.1016/j.ophtha.2016.04.044 View in Article
- Clinical utility of intraocular pressure monitoring outside of normal office hours in patients with glaucoma. Arch Ophthalmol. Jun. 2006; 124: 793https://doi.org/10.1001/archopht.124.6.793 View in Article
- Meeting an unmet need in glaucoma: continuous 24-h monitoring of intraocular pressure. Expert Rev Med Devices. May 2012; 9: 225-231https://doi.org/10.1586/erd.12.14 View in Article
- Can the SENSIMED Triggerfish ® lens data be used as an accurate measure of intraocular pressure?. Acta Ophthalmol. Mar. 2018; 96: e242-e246https://doi.org/10.1111/aos.13456 View in Article
- Device profile of the EYEMATE-IOTM system for intraocular pressure monitoring: overview of its safety and efficacy. Expert Rev Med Devices. Jun. 2020; 17: 491-497https://doi.org/10.1080/17434440.2020.1761788 View in Article
- Telemetric measurement of intraocular pressure via an implantable pressure sensor—12-month results from the ARGOS-02 trial. Am J Ophthalmol. Jan. 2020; 209: 187-196https://doi.org/10.1016/j.ajo.2019.09.011 View in Article
-
- Read S.A.
- Collins M.J.
- Measurement of the difference in intraocular pressure between the sitting and lying body positions in healthy subjects: direct comparison of the Icare Pro with the Goldmann applanation tonometer, Pneumatonometer and Tonopen XL. Clin Exp Ophthalmol. Sep. 2014; 42: 608-614https://doi.org/10.1111/ceo.12272 View in Article
- The influence of soft contact lenses on the intraocular pressure measurement. Eye. Feb. 2012; 26: 278-282https://doi.org/10.1038/eye.2011.271 View in Article
- 24-hour intraocular pressure fluctuation monitoring using an ocular telemetry sensor. J Glaucoma. Oct. 2012; 21: 539-544https://doi.org/10.1097/IJG.0b013e31821dac43 View in Article
- Continuous IOP fluctuation recording in normal tension glaucoma patients. Curr Eye Res. Dec. 2011; 36: 1129-1138https://doi.org/10.3109/02713683.2011.608240 View in Article
- 24-hour monitoring of intraocular pressure fluctuations using a contact lens sensor: diagnostic performance for glaucoma progression. Investigative Opthalmology & Visual Science. Mar. 2023; 64: 3https://doi.org/10.1167/iovs.64.3.3 View in Article
- Association of ultra-short-term intraocular pressure fluctuation with disease progression in primary angle closure glaucoma: the CUPAL study. J Glaucoma. Nov. 2022; 31: 874-880https://doi.org/10.1097/IJG.0000000000002103 View in Article
- The effect of daily life activities on intraocular pressure related variations in open-angle glaucoma. Sci Rep. Mar. 2021; 11: 6598https://doi.org/10.1038/s41598-021-85980-2 View in Article
- Diurnal spikes of intraocular pressure in uveitic glaucoma: A 24-hour intraocular pressure monitoring study. Semin Ophthalmol. May 2020; 35: 246-251https://doi.org/10.1080/08820538.2020.1809683 View in Article
- Intereye symmetry of 24-hour intraocular pressure–related patterns in untreated glaucoma patients using a contact lens sensor. J Glaucoma. Aug. 2020; 29: 666-670https://doi.org/10.1097/IJG.0000000000001563 View in Article
- Twenty-four–hour intraocular pressure-related patterns from contact lens sensors in normal-tension glaucoma and healthy eyes. Ophthalmology. Nov. 2020; 127: 1487-1497https://doi.org/10.1016/j.ophtha.2020.05.010 View in Article
- Using 24-hr ocular dimensional profile recorded with a sensing contact lens to identify primary open-angle glaucoma patients with intraocular pressure constantly below the diagnostic threshold. Acta Ophthalmol. 2020; 98: Dechttps://doi.org/10.1111/aos.14453 View in Article
- Can a contact lens sensor predict the success of trabectome surgery?. Graefe’s Archive for Clinical and Experimental Ophthalmology. Apr. 2020; 258: 843-850https://doi.org/10.1007/s00417-019-04576-9 View in Article
- Influence of ocular dimensional change on 24-hour intraocular pressure measurement with contact lens sensor. J Glaucoma. Sep. 2019; 28: 808-810https://doi.org/10.1097/IJG.0000000000001318 View in Article
- Evaluation of the 24-hour intraocular pressure and systemic blood pressure at the same time. J Fr Ophtalmol. Sep. 2019; 42: 739-745https://doi.org/10.1016/j.jfo.2019.03.007 View in Article
- The influence of electromagnetic radiation on the measurement behaviour of the triggerfish® contact lens sensor. BMC Ophthalmol. Dec. 2018; 18: 338https://doi.org/10.1186/s12886-018-1013-x View in Article
artículo traducido por opticos-optometristas.com del artículo original A first-in-human pilot study of a novel electrically-passive metamaterial-inspired resonator-based ocular sensor embedded contact lens monitoring intraocular pressure fluctuations


















_1400_large.jpeg)